Regulatory News:
Ce communiqué de presse contient des éléments multimédias. Voir le communiqué complet ici : https://www.businesswire.com/news/home/20181111005032/fr/
(Graphic: Business Wire)
VALBIOTIS (FR0013254851 – ALVAL / éligible PEA/PME), entreprise française de Recherche & Développement engagée dans l’innovation scientifique, pour la prévention et la lutte contre les maladies métaboliques, annonce un nouveau champ d’application pour VALEDIA®, étendu à la prévention de la NASH2. Ce nouveau champ d’application est basé sur un ensemble de résultats révélés aujourd’hui qui démontrent le potentiel clinique pour la réversion de la stéatose hépatique non alcoolique, en prévention de la NASH. Ils permettent le lancement d’études cliniques de Phase II sur cet objectif, en complément des études en cours pour la réduction du risque de diabète de type 2. Ce nouveau champ d’application conforte VALEDIA® dans son statut de produit précurseur pour de nouvelles stratégies de prévention des maladies métaboliques sévères, spécifiquement centrées sur les facteurs de risque de ces maladies. En complément du prédiabète, VALEDIA® serait le premier produit destiné aux sujets présentant une stéatose hépatique, stade précoce des atteintes métaboliques du foie ou NAFLD3, en amont des stades sévères comme la NASH. On estime aujourd’hui que ces atteintes métaboliques affectent 25% de la population mondiale et sont en pleine expansion4.
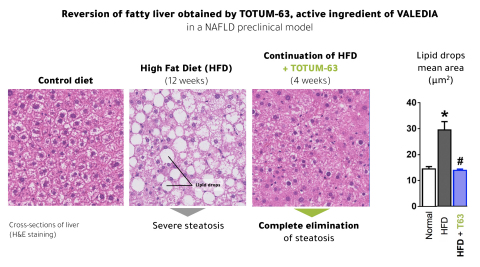
Des investigations menées par l’Université de Leiden (Pays-Bas) dans le cadre d’un partenariat scientifique ont démontré une réversion complète de la stéatose hépatique par le principe actif de VALEDIA®, TOTUM-63, dans un modèle in vivo de NAFLD.
En parallèle, des études in vivo mettent en évidence un mécanisme d’action de TOTUM-63 sur 3 cibles cellulaires clés de la physiopathologie de la stéatose hépatique non alcoolique : les facteurs de transcription Ppar ß/∂, FXR et la protéine Fsp27. L’ensemble de l’étude détaille ce mécanisme d’action pour la prévention des atteintes métaboliques du foie et est actuellement présenté au congrès de l’American Association for the Study of Liver Diseases (AASLD), du 9 au 13 novembre 2018 à San Francisco (poster n°1827F).
Enfin, des résultats additionnels de l’étude clinique de Phase I/II réalisée sur TOTUM-63 en 2017, non communiqués à ce jour, montrent une amélioration du bilan lipidique, incluant une réduction des taux sanguins de cholestérol et de triglycérides. Ces résultats sur le profil lipidique renforcent les données positives déjà obtenues sur l’insulino-sensibilité. Les altérations du profil lipidique et la résistance à l’insuline sont reconnues pour leur forte implication dans l’apparition et la progression de la stéatose hépatique.
Révélé pour la première fois aujourd’hui, cet ensemble de résultats est issu du programme de recherche mené jusqu’ici sous le nom de VAL-63 NAFLD.
VALEDIA®, un produit global pour la prévention du diabète de type 2 et de la NASH dès 2021
Une fois le développement clinique achevé chez les sujets prédiabétiques, VALEDIA® pourra être mis sur le marché avec une allégation de santé relative à la réduction du risque de diabète de type 2 à l’horizon 2021. Au-delà de cette indication initiale, dès sa commercialisation, VALEDIA® pourrait aussi être recommandé par les professionnels de santé à des sujets présentant une stéatose hépatique sans prédiabète. Cette recommandation pourrait être faite sur la base des premières données cliniques issues du développement de VALEDIA® sur la stéatose.
Dans un second temps, l’obtention d’une allégation de santé spécifique, pour la réduction de la stéatose hépatique et la réduction du risque de NASH, sera visée dès 2023. Elle permettra de répondre aux besoins de l’ensemble de cette population stéatosique sans prédiabète, estimée selon la Société à 13,3% de la population générale aux USA et 4,5% en Europe.
Le modèle d’affaires envisagé pour VALEDIA® est un accord de licence avec un ou plusieurs acteurs de la santé en fonction des zones géographiques comprenant un paiement initial (upfront), des versements d’étapes et des redevances sur les ventes.
Le développement clinique de Phase II de VALEDIA® pour la réduction du risque de NASH débutera par une étude de Phase IIA, randomisée et contrôlée contre placebo. Elle devrait être lancée en 2019 dans une population cible présentant une stéatose hépatique non alcoolique, avec la réduction de la stéatose comme critère principal. La stéatose initiale et son évolution seront évaluées par une méthode non-invasive.
Le Pr Samy HADJADJ, diabétologue et endocrinologue au CHU de Nantes, commente : « NAFLD et NASH sont des pathologies aujourd’hui fréquemment retrouvées chez les personnes souffrant d’une maladie métabolique déclarée ou d’un désordre métabolique liés à l’insulino-résistance. Compte tenu du pronostic particulièrement sombre de la NASH, sans traitement établi à ce jour mis à part la transplantation hépatique au stade le plus avancé, il y a un réel besoin de prévention, dès le stade stéatosique, pour réduire efficacement le contenu en graisse du foie. Sur ce critère, les résultats de VALEDIA® obtenus jusqu’ici sont hautement prometteurs, en permettant une correction de la stéatose malgré la poursuite du régime riche en graisse. Si ce résultat expérimental est validé par des études cliniques chez l’Homme, VALEDIA® pourrait constituer un véritable recours pour des personnes à risque de développer une NASH. »
Sébastien PELTIER, Président du Directoire de Valbiotis, précise : « VALEDIA® prend aujourd’hui une nouvelle dimension, tant les données divulguées sont cohérentes pour la réversion de la stéatose hépatique. Ce challenge est ambitieux : nous faisons le choix de le relever car nous disposons d’un produit dont le potentiel est au rendez-vous, avec un mécanisme d’action enthousiasmant, des données précliniques incontestables et de premiers indices cliniques encourageants. Ce nouveau développement pour VALEDIA® donne à ce produit pionnier un positionnement global pour la prévention, dans le domaine élargi des maladies métaboliques liées à l’insulino-résistance. VALEDIA® porte aujourd’hui une promesse unique et forte : devenir le « backbone » de la prévention des maladies métaboliques et couvrir les besoins d’une large population à risque de développer un diabète de type 2 et/ou une NASH. »
Le détail des nouveaux résultats annoncés de TOTUM-63, principe actif de VALEDIA®, sur la stéatose hépatique non alcoolique
1. Une réversion complète de la stéatose hépatique, dans des modèles de stéatose déjà déclarée
Dans le cadre d’un partenariat de recherche avec l’Université de Leiden, une étude évaluait l’efficacité de TOTUM-63 dans un modèle in vivo ayant préalablement développé une forte stéatose du foie. Dans cette étude de « réversion », l’adjonction du principe actif de VALEDIA® a restauré en 4 semaines un état hépatique non stéatosique. La disparition de la stéatose était démontrée par des analyses histologiques et associée au retour de la sensibilité à insuline (indice HOMA-IR) à des valeurs contrôle.
Bruno GUIGAS, chercheur et Professeur assistant à l’Université de Leiden (Pays-Bas) a mené cette étude et détaille ces résultats : « Nous avons conduit des analyses sur l’ensemble des paramètres histologiques, biochimiques et physiologiques de la stéatose hépatique : toutes convergent vers une démonstration d’efficacité très significative de TOTUM-63 pour la réversion de la stéatose. À ce stade de développement, les résultats sont incontestables et même assez spectaculaires. »
2. Un mécanisme d’action sur 3 cibles cellulaires essentielles, en prévention de la stéatose hépatique
Dans un modèle in vivo de NAFLD, la complémentation par TOTUM-63 simultanément à la prise d’un régime riche en graisses pendant 16 semaines a prévenu l’apparition d’une forte stéatose hépatique, observée dans les modèles non complémentés. L’étude du mécanisme d’action du principe actif a révélé une augmentation significative de l’expression génique de Ppar ß/∂ (multipliée par 3) et FXR (+ 30%), deux facteurs de transcription clés du métabolisme énergétique hépatique. En parallèle, TOTUM-63 inhibe quasi totalement l’expression génique de la protéine Fsp27, qui régule le stockage des lipides et s’exprime spécifiquement dans le foie stéatosique.
Ce mécanisme d’action focalisé sur le contrôle du métabolisme hépatique constitue un atout fort contre la stéatose hépatique et pour la réduction du risque de NASH, dès les stades précoces.
3. Chez l’Homme, une amélioration significative du profil lipidique, portant sur la cholestérolémie totale et la triglycéridémie
L’étude clinique de Phase I/II réalisée en 2017 sur TOTUM-63, principe actif de VALEDIA®, avait déjà confirmé chez l’Homme sain une amélioration de la sensibilité à l’insuline. De nouveaux résultats sur le profil lipidique, non encore communiqués à ce jour, ont montré une réduction significative des taux sanguins de cholestérol total (-5,5%) et de triglycérides (-18,5%) dès la première dose testée de 2,5 g/jour. Aucune élévation du taux sanguin de LDL-cholestérol n’était observée (-7,3% à 2,5 g/jour , p=0,07 ; -7,4% à 5 g/jour, p=0,08), alors qu’il s’agit d’un événement indésirable déjà rencontré pour un principe actif agissant sur la voie FXR. L’insulino-résistance et la dyslipidémie sont reconnues pour être fortement associés au développement de la stéatose hépatique puis de la NASH.
À propos des NAFLDs
Un large besoin de prévention contre l’épidémie des NAFLDs
À l’échelle mondiale, la prévalence des NAFLDs serait supérieure à 25%4. Selon les estimations, elles toucheraient entre 50 et 70% des patients diabétiques5, 60 à 75% des sujets obèses et 50% des sujets dyslipidémiques6. Corrélé à la pandémie de diabète et d’obésité, le nombre de cas est en constante augmentation dans les pays industrialisés : les projections anticipent une croissance de + 21% pour la stéatose hépatique non-alcoolique et de + 63% pour la NASH à l’horizon 20307.
Le Fatty Liver Index : un suivi de la stéatose hépatique réalisable en routine par le médecin traitant
Une des difficultés pour l’évaluation clinique de ces atteintes du foie réside dans le recours nécessaire à la biopsie hépatique. Néanmoins, des scores basés sur des examens courants existent et présentent l’avantage d’être facilement réalisables en médecine générale. C’est le cas du Fatty Liver Index (FLI), calculé à partir de 4 mesures réalisées en routine : le taux sanguin de triglycérides, l’Indice de Masse Corporelle, le dosage sanguin des Gamma Glutamyl Transférases (GGT) et la mesure du tour de taille. Le FLI peut constituer un marqueur indirect de la stéatose hépatique et être utilisé pour le dépistage et le suivi des patients chez qui la stéatose est suspectée8. Des techniques non-invasives d’imagerie sont également disponibles et présentent l’avantage d’être peu coûteuses et réitérables9.
La NASH : une forme sévère et avancée de la stéatose hépatique
La stéatose hépatique correspond à une accumulation de graisses dans les cellules du foie. Dans la NASH, elle se complique d’une inflammation et de lésions tissulaires. D’un pronostic souvent sombre, – 38% de survie à 10 ans, la NASH peut évoluer vers une fibrose et une cirrhose, à l’origine d’une insuffisance hépatique et, dans certains cas, d’un cancer du foie10.
Les études disponibles estiment que 40% des personnes atteintes de stéatose hépatique évolueront ainsi vers une NASH11. Cette stéatose hépatique est considérée comme un état à risque de développer une NASH12.
A PROPOS DE VALBIOTIS
VALBIOTIS est une entreprise française de Recherche & Développement engagée dans l’innovation scientifique, pour la prévention et la lutte contre les maladies métaboliques. Ses produits sont destinés aux industriels de l’agro-alimentaire, et de l’industrie pharmaceutique. VALBIOTIS intervient notamment pour la prévention du diabète de type 2, de la NASH (stéatohépatite non-alcoolique), de l’obésité et des pathologies cardiovasculaires.
Créée début 2014 à La Rochelle, l’entreprise a noué de nombreux partenariats avec des centres académiques d’excellence en France et à l’étranger, dont l’Université de la Rochelle, le CNRS, et l’Université Clermont Auvergne située à Clermont-Ferrand. Ces accords lui permettent de bénéficier depuis sa création d’un fort effet de levier grâce notamment à des experts et partenaires techniques mobilisés sur ses projets. L’Entreprise est installée sur 3 sites en France – Périgny, La Rochelle (17) et Riom (63) – auxquels s’ajoute un bureau américain à Boston (MA).
Membre du réseau « BPI Excellence » et bénéficiant du label BPI « Entreprise Innovante », VALBIOTIS dispose aussi du statut « Jeune Entreprise Innovante » et a obtenu un appui financier important de l’Union Européenne pour ses programmes de recherche via l’obtention de Fonds Européen de Développement Économique Régional (FEDER).
Toute l’information sur VALBIOTIS :
http
://valbiotis.com/
Nom : VALBIOTIS
Code ISIN : FR0013254851
Code Mnémonique :
ALVAL
_____________________________
1 Étude réalisée par
l’Université de Leiden (Pays-Bas) sur des modèles murins de NAFLD
2
NASH : Non Alcoholic Stetohepatitis, équivalent anglais de
stéatohépatite non alcoolique
3 NAFLD : Non-Alcoholic
Fatty Liver Disease, équivalent anglais d’hépatopathie non alcoolique
4
Younossi Z.M. et al. Hepatology, 2016
5 Anstee, Targher
et al. 2013
6 Assy, Kaita et al. 2000
7
Estes C. et al., Hepatology, 2018
8 Bedogni G., BMC
Gastroenterology, 2006
9 Papagianni M et al. World J
Hepatol 2015;7(4):638-648
10 World Gastroenterology
Organisation Global Guidelines. Non-alcoholic Fatty Liver Disease and
Non-alcoholic Steatohepatitis. http://www.worldgastroenterology.org/assets/export/userfiles/2012_NASH%20and%20NAFLD_Final_long.pdf
11
McPherson S et al. J Hepatol 2015;62(5):1148-55
12
Vizuete J et al. J Clin Transl Hepatol 2017;5(1):67-75
Consultez la version source sur businesswire.com : https://www.businesswire.com/news/home/20181111005032/fr/


