Poxel précoce. Le laboratoire a (déjà) dégainé son rapport financier du 1er trimestre 2019. Poxel affichait 59 millions d'euros de trésorerie et équivalents fin mars dernier, contre 66,7 millions d'euros trois mois avant. Les revenus trimestriels se sont élevés à 14,9 millions d'euros, issus du partenariat avec Sumitomo Dainippon Pharma. La société doit présenter rapidement ("au début du deuxième trimestre") les résultats de la phase III TIMES1 avec l’Imeglimine, puis à mi-année les résultats intermédiaires de TIMES3. Il faudra attendre la fin d'exercice pour prendre connaissance des données de TIMES2 et des résultats complémentaires de TIMES3. En parallèle, Poxel et Sumitomo Dainippon Pharma préparent le dossier d'enregistrement au Japon dans le diabète de type 2.
GKT831 à vienne. Genkyotex profite de l'ILC 2019 de Vienne (du 10 au 14 avril) pour présenter des résultats d'efficacité intermédiaires tirés de la phase II avec GKT831 dans la cholangite biliaire primitive. Un abstract a été retenu pour une présentation orale le 11 avril. La société traité 111 patients pendant 24 semaines. Les résultats finaux de l'essai à 24 semaines sont attendus d'ici la fin du printemps (la date de collecte d'information auprès du dernier patient traité est justement fixée au 11 avril, selon les données officielles).
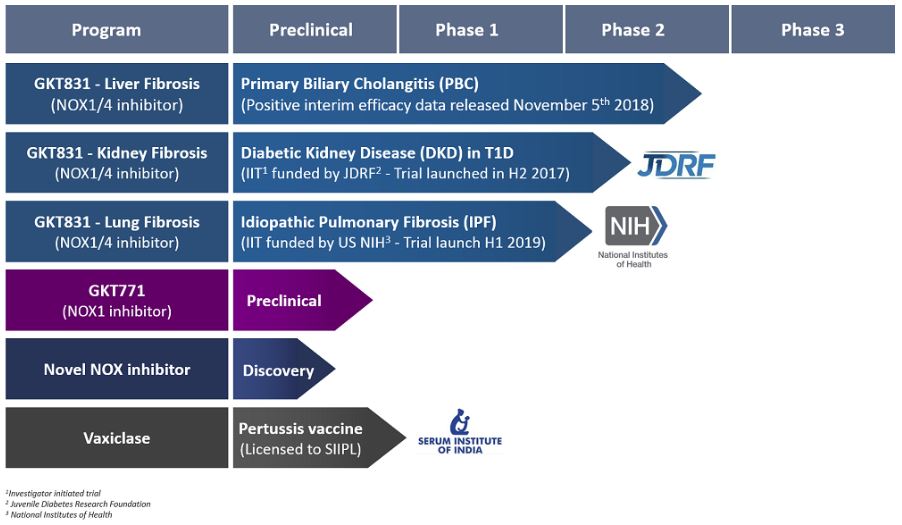
Le portefeuille de Genkyotex (Source Société)
Sanofi ajuste son accord avec Alnylam. Les deux entreprises ont mis un terme au volet "Recherche et Options" de l'alliance scellée en 2014 autour des agents thérapeutiques ARNi pour le traitement de maladies génétiques rares. Les principales modalités concernant le patisiran, le vutrisiran et le fitusiran ne varient pas. En revanche, Alnylam va développer un agent expérimental supplémentaire pour le traitement d'une maladie génétique rare tenue secrète, jusqu'aux études pouvant permettre d'envisager le dépôt d'une demande de nouveau médicament expérimental. Le Français se chargera de la poursuite potentielle du développement et de la commercialisation. Alnylam serait alors éligible à des redevances à deux chiffres sur les ventes mondiales. Le duo a aussi modifié "certaines modalités du contrat de prise de participation de Sanofi au capital d'Alnylam, de manière à donner à Sanofi la possibilité de lever l'engagement de conservation des titres Alnylam en sa possession, sous réserve de certaines restrictions sur leur négociation entres autres dispositions". Mais sans donner plus de détails.
En bref. Onxeo a mis en ligne les documents réglementaires en vue de son assemblée générale du 26 avril. Néovacs a publié son calendrier de communication financière 2019.

 Par
Par 













