Selon une analyse menée auprès de plus de 2 000 patients d'une importante base de données américaine, les patients ayant subi une ICP à haut risque non urgente réalisée à l'aide de la pompe cardiaque Impella (n=1 447) présentaient une survie nettement améliorée, une réduction des infarctus du myocarde, une réduction du choc cardiogénique après l'ICP ainsi qu'une durée de séjour réduite par rapport aux patients du même groupe traités à l'aide d'une pompe à ballonnet intra-aortique (PBIA) (n=709). Les conclusions de l'étude confortent et renforcent les résultats d'autres études contrôlées par des pairs au cours des dix dernières années.
Ce communiqué de presse contient des éléments multimédias. Voir le communiqué complet ici : https://www.businesswire.com/news/home/20221013005351/fr/
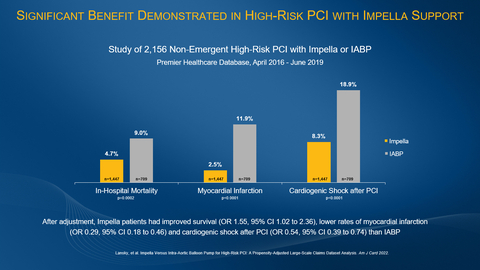
Figure 1 (Graphic: Business Wire)
L'étude a été publiée le 7 octobre dans The American Journal of Cardiology. Elle a été réalisée par un groupe de médecins-chercheurs experts, sous la direction d'Alexandra Lansky, DM, professeure de médecine à la Yale School of Medicine et cardiologue praticienne au Yale-New Haven Hospital. La Dre Lansky dirige également le Yale Heart and Vascular Clinical Research Program et le Yale Cardiovascular Research Center, spécialisé dans l'évaluation des dispositifs d'intervention.
"Cette étude réalisée sur la base d'une grande base de données contemporaine en conditions réelles démontre une fois encore les avantages de l'utilisation d'Impella dans le cadre d'une ICP à haut risque afin de stabiliser l'hémodynamique, d'empêcher l'effondrement hémodynamique, de permettre une revascularisation optimale et d'améliorer les résultats cliniques", a déclaré la Dre Lansky.
L'étude a analysé les patients de la base de données Premier Healthcare traités entre 2016 et 2019 avec Impella ou PBIA pour une ICP à haut risque non urgente. Les patients ont été appariés selon des méthodes de score de propension permettant de contrôler les différences de base, de procédure et de traitement médical post-ICP entre les groupes. L'étude a révélé les éléments suivants :
- La survie en milieu hospitalier était significativement supérieure avec Impella par rapport à la PBIA (95,3 % contre 91,0 % non ajustés, p=0,0002 ; odds ratio (OR) ajusté 1,55, intervalle de confiance à 95 % (IC) 1,02, 2,36, p=0,042).
- L'infarctus du myocarde a diminué de manière significative avec Impella par rapport à la PBIA (2,5 % non ajusté contre 11,9 %, p<0,0001 ; odds ratio ajusté 0,29, IC à 95 % 0,18, 0,46, p<0,0001).
- Le choc cardiogénique après une ICP était nettement inférieur avec Impella par rapport à la PBIA (8,3 % vs. 18,9 % p<0,0001 ; OR ajusté 0,54, IC 95 % 0,39, 0,74, p=0,0001).
- Une hospitalisation réduite pour les patients Impella par rapport aux patients PBIA (3,1 jours non ajusté vs. 5,5 jours, p<0,0001 ; 3,4 jours ajusté vs. 4,8 jours, p<0,0001).
Par ailleurs, le profil sécuritaire lié aux hémorragies et aux accidents vasculaires cérébraux était similaire dans les groupes Impella et PBIA. Ces résultats sont cohérents avec les données attestant d'une amélioration des hémorragies au fil du temps pour les dispositifs à gros calibre, compte tenu de l'adoption de pratiques contemporaines telles que l'accès vasculaire guidé par échographie et l'utilisation optimale des dispositifs de fermeture. (voir figure 2)
Les auteurs de Lansky et al. ont étudié les données récentes des organismes payeurs pour les années qui ont suivi l'approbation d'Impella par la FDA pour les ICP à haut risque, alors même que les meilleures pratiques d'utilisation d'Impella avaient été établies. Ils ont en outre appliqué une méthode d'appariement par propension plus directe que les études antérieures réalisées à partir d'ensembles de données similaires.
Les résultats de Lansky et al. confirment et complètent les résultats d'autres études sur Impella dans l'ICP à haut risque, notamment l'essai contrôlé randomisé (ECR) PROTECT II, l'étude PROTECT III et l'étude RESTORE EF. L'étude PROTECT II a établi que l'utilisation d'Impella entraînait une réduction de 29 % du risque relatif d'évènement indésirable cardiaque (MACCE) à 90 jours par rapport à la PBIA. L'étude PROTECT III a permis de constater une nouvelle amélioration des résultats cliniques à 90 jours, de la plénitude de la revascularisation et de la sécurité par rapport à l'ECR PROTECT II. (voir figure 3) Restore EF a fait apparaître que l'utilisation des meilleures pratiques contemporaines avec Impella dans les ICP à haut risque améliore considérablement la fraction d'éjection ventriculaire gauche (FEVG), les symptômes d'insuffisance cardiaque ainsi que les symptômes angineux à 90 jours de suivi chez des patients traités dans divers environnements hospitaliers, notamment des centres médicaux ruraux, urbains, communautaires et universitaires. (voir figures 4 et 5)
À PROPOS DES POMPES CARDIAQUES IMPELLA
L'Impella 2.5® et l'Impella CP® avec SmartAssist® sont approuvés par la FDA américaine pour traiter certains patients atteints d'insuffisance cardiaque avancée subissant des interventions coronariennes percutanées (ICP) électives et urgentes, telles que la pose d'un stent ou l'angioplastie par ballonnet, pour rouvrir les artères coronaires bloquées.
À PROPOS D'ABIOMED
Basé à Danvers, Massachusetts, États-Unis, Abiomed (Nasdaq: ABMD) est un fournisseur de technologie médicale leader du marché qui fournit des solutions d’assistance circulatoire et d’oxygénation. Nos produits sont conçus pour permettre au cœur de se reposer en améliorant le flux sanguin et/ou en fournissant une oxygénation suffisante aux personnes souffrant d'insuffisance respiratoire. Pour plus d'informations, rendez-vous sur : abiomed.com.
DÉCLARATIONS PROSPECTIVES
Toute déclaration prospective est soumise à des risques et incertitudes tels que ceux décrits dans les rapports périodiques d'Abiomed déposés auprès de la Securities and Exchange Commission. Les résultats réels peuvent différer sensiblement des résultats prévus.
Le texte du communiqué issu d’une traduction ne doit d’aucune manière être considéré comme officiel. La seule version du communiqué qui fasse foi est celle du communiqué dans sa langue d’origine. La traduction devra toujours être confrontée au texte source, qui fera jurisprudence.
Consultez la version source sur businesswire.com : https://www.businesswire.com/news/home/20221013005351/fr/

